برگرفته از: National Metallurgical Laboratory
مترجم: پریسا آتشی
فسفاته کردن یکی از فرایندهای پیشعملی متداول برای آمادهسازی سطح فلزات آهنی و غیرآهنی جهت عملیات بعدی مانند پوششدهی و پرداختکاری است. به دلیل اقتصادی بودن، سرعت بالای عملیات و توانایی ایجاد مقاومت عالی در برابر خوردگی، سایش، چسبندگی و روانکاری، این فرایند نقش مهمی در صنایع خودرو، فرآیند و لوازم خانگی ایفا میکند. اگرچه این فرایند در ابتدا بهعنوان یک روش ساده برای جلوگیری از خوردگی توسعه یافت، اما تغییرات در کاربردهای نهایی محصولات فسفاته شده، اصلاح فرایندهای موجود و توسعه روشهای نوآورانه برای جایگزینی روشهای سنتی را ضروری کرده است. برای همگامی با نیازهای سریعاً در حال تغییر سیستمهای پرداختکاری، اصلاحات متعددی در توسعه این فرایندها صورت گرفته است، هم در توالی فرآیند و هم در فرمولاسیونهای فسفاته کردن. این بررسی به جنبههای مختلف فسفاته کردن بهطور مفصل میپردازد. با وجود اصلاحات متعدد در فناوریهای رسوبگذاری برای دستیابی به انواع مختلف پوششها و خواص مطلوب مانند بهبود مقاومت به خوردگی، مقاومت به سایش و غیره، پوششهای تبدیلی فسفات همچنان نقش حیاتی در صنایع خودرو، فرآیند و لوازم خانگی ایفا میکنند.
فلزات ستون فقرات تمدن بشری بوده اند. تلاشهای فراوانی برای یافتن جایگزینهایی برای فلزات انجام شده است، اما این مواد همچنان نقش اصلی را در تولید و ساختوساز ایفا میکنند و احتمالاً برای سالهای متمادی این نقش را حفظ خواهند کرد. این به دلیل ترکیبی از چندین ویژگی مفید مانند استحکام، قابلیت شکلپذیری، هزینه پایین و قابلیت بازیافت است که فلزات از آن برخوردارند. با این حال، فلزاتی که از طریق روشهای شیمیایی یا الکتروشیمیایی از سنگ معدن استخراج میشوند، تمایل شدیدی به بازگشت به شکل اکسید خود در اولین فرصت ممکن را نشان میدهند، یعنی تمایل به خوردگی دارند [1-4] و در نتیجه، علاوه بر ایجاد خسارات اقتصادی هنگفت، تهدیدی جدی برای منابع ملی یک کشور محسوب میشوند.
روشهای جلوگیری از خوردگی متعدد و متنوع هستند. این روشها را میتوان به طور کلی به شرح زیر طبقهبندی کرد [3]:
رایجترین روش محافظت در برابر خوردگی شامل آلیاژسازی حجمی یا اصلاح سطح است. با این حال، اصلاح سطح بسیار اقتصادیتر از آلیاژسازی حجمی است و به طور گستردهتری مورد استفاده قرار میگیرد. روشهای معمولاً مورد استفاده برای اصلاح سطح شامل تشکیل یک مانع فیزیکی برای محافظت از فلز در برابر محیط خورنده است [5]. این امر را میتوان با روشهای نسبتاً مدرنتری مانند: (i) رسوبدهی فیزیکی بخار (PVD)؛ (ii) رسوبدهی شیمیایی بخار (CVD)؛ (iii) کاشت یونی؛ (iv) فرآوری لیزری؛ (v) رسوبدهی با اسپری حرارتی، اسپری پلاسما و روشهای قوس الکتریکی؛ (vi) نیتراسیون؛ (vii) کاربیداسیون؛ و غیره، یا از طریق تکنیکهای سنتیتر مانند: (i) رنگآمیزی؛ (ii) آندیزاسیون؛ و (iii) پوششهای تبدیل شیمیایی، انجام داد.
در حالی که روشهای اول معمولاً کمتر اقتصادی هستند زیرا شامل استفاده از تکنیکهای کاربرد پیچیده هستند و برای کاربردهای تخصصی در نظر گرفته شدهاند، روشهای اخیر مقرونبهصرفهتر هستند و طیف گستردهتری از کاربردهای نهایی را دارند.
پوششهای تبدیل شیمیایی، فیلمهای سطحی غیرقابل انحلال، غیرآلی، بلوری یا آمورف چسبندهای هستند که به عنوان بخشی جداییناپذیر از سطح فلز از طریق یک واکنش شیمیایی غیرالکترولیتی بین سطح فلز و محلول غوطهوری تشکیل میشوند [6]. در چنین پوششهایی، بخشی از فلز پایه به یکی از اجزای فیلم محافظ حاصل تبدیل میشود که بسیار کمتر از سطح فلز اصلی در برابر خوردگی بعدی واکنشپذیر است. این فیلم پتانسیل یکسانی را به سطح فلز میدهد و پتانسیل محلهای خوردگی گالوانیک آندی و کاتدی محلی را خنثی میکند [7].
آنها همچنین به عنوان پایههای جاذب برای بهبود چسبندگی به رنگها و سایر پوششهای آلی عمل میکنند. پوششهای تبدیل شیمیایی به دلیل ماهیت چسبنده و سرعت بالای تشکیل پوشش، علاوه بر اقتصادی بودن، ترجیح داده میشوند. علاوه بر این، میتوان آنها را با استفاده از تجهیزات ساده و بدون اعمال هیچ پتانسیل خارجی تشکیل داد. فرآیندهای پوششدهی تبدیل شیمیایی بر اساس اجزای اصلی خود به فسفاته کردن، کروماته کردن و اگزالات کردن طبقهبندی میشوند که به ترتیب فسفاتها، کروماتها و اگزالاتها هستند [8]. این بررسی بر روی پوششهای تبدیل فسفات با تأکید ویژه بر پوششهای فسفات روی بر روی فولاد ملایم متمرکز است.
فرآیند فسفاته کردن را میتوان به عنوان فرآیند تیمار سطح فلز برای ایجاد یک پوشش سطحی غیر رسانای الکتریکی، نسبتاً سخت و نامحلول از فسفات تعریف کرد که با فلز زیرین پیوسته و بسیار چسبنده است و جذبپذیری بیشتری نسبت به فلز دارد [9]. این پوشش در نتیجه یک واکنش توپوشیمیایی تشکیل میشود که باعث میشود سطح فلز پایه خود را به عنوان بخشی از فیلم مقاوم در برابر خوردگی ادغام کند.
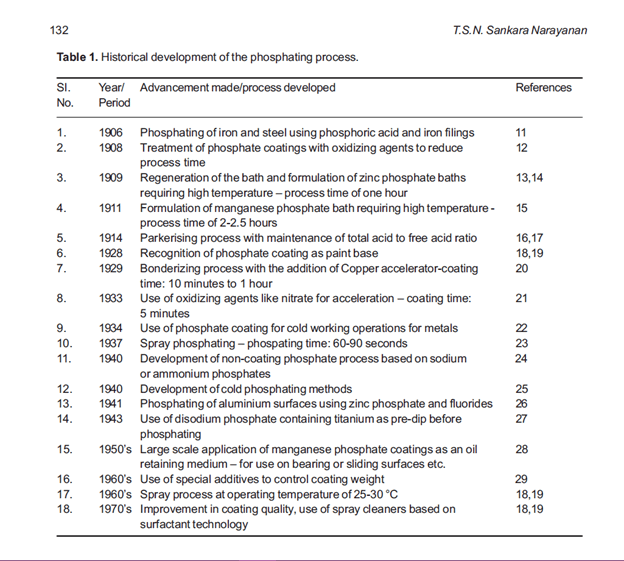
استفاده از پوششهای فسفات برای محافظت از سطوح فولادی از ابتدای قرن بیستم شناخته شده است و در این دوره، بخش عمدهای از تولید جهانی خودرو، یخچال و مبلمان به این روش پوشش داده میشد. اولین سند معتبر در مورد استفاده از پوششهای فسفات برای جلوگیری از زنگزدگی آهن و فولاد، پتنت بریتانیایی سال 1869 است که به روس اعطا شد [10]. در روش مورد استفاده توسط او، قطعات آهن داغ شده در اسید فسفریک غوطهور میشدند تا از زنگزدگی جلوگیری شود. از آن زمان تاکنون، پیشرفتهای متعددی صورت گرفته است که مهمترین آنها در جدول 1 فهرست شده است.
در طول 30 سال گذشته، کارها عمدتاً بر روی بهبود کیفیت، به ویژه برای همگام شدن با نیازهای متغیر اخیر سیستمهای پوششدهی آلی، متمرکز شده است. از جمله مهمترین این پیشرفتها میتوان به موارد زیر اشاره کرد: (i) استفاده از حمامهای فسفاته کردن با دمای پایین برای غلبه بر بحران انرژی [30-32]؛ (ii) استفاده از فناوری روی کم [18،19]؛ (iii) استفاده از افزودنیهای ویژه در حمام فسفاته [33-42]؛ (iv) استفاده از بیش از یک یون فلز سنگین در ترکیب موجود – به ویژه فسفاته کردن سه کاتیونی [43]؛ و غیره. انواع جدیدی از پوششهای فسفات مانند پوششهای فسفات قلع، نیکل و سرب معرفی شدهاند [44،45] علاوه بر توسعه ترکیبات برای فسفاته کردن همزمان چندین زیرلایه فلزی [46،47]. استفاده از جایگزینهای شستشوی نهایی کروم (VI) متداول [48] برای تطابق با مقررات اعمال شده توسط مقامات کنترل آلودگی بر استفاده از ترکیبات کروم (VI) رو به افزایش است.
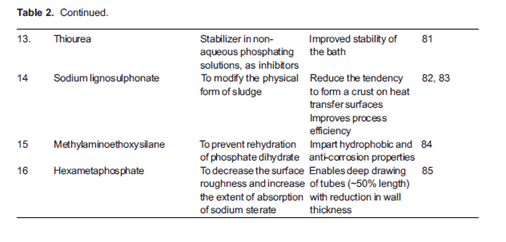
افزودنیهای ویژه مورد استفاده در حمامهای فسفاته در جدول 2 و جایگزینهای شستشوی نهایی کروم (VI) در جدول 3 ارائه شده است.

.
همه محلولهای فسفاته کردن متداول، محلولهای رقیق اسید فسفریک هستند که حاوی یک یا چند یون فلز قلیایی/فلز سنگین هستند و اساساً حاوی اسید فسفریک آزاد و فسفاتهای اولیه یونهای فلزی موجود در حمام هستند [18،19،24،127،128]. هنگامی که یک پنل فولادی وارد محلول فسفاته کردن میشود، یک واکنش توپوشیمیایی رخ میدهد که در آن انحلال آهن در میکروآندهای موجود روی زیرلایه توسط اسید فسفریک آزاد موجود در حمام آغاز میشود. در میکروکاتدها، هیدروژن آزاد میشود.
Fe + 2H3PO4 ® Fe(H2PO4)2 + H2 . (1)
تشکیل فسفات آهن اولیه محلول منجر به کاهش همزمان غلظت اسید آزاد در محلول میشود که در نتیجه افزایش pH در محلول/رابطه فلزی میشود. این تغییر در pH تعادل هیدرولیز بین فسفاتهای اولیه محلول و فسفاتهای سوم نامحلول یونهای فلز سنگین موجود در محلول فسفاته را تغییر میدهد که منجر به تبدیل سریع و رسوب فسفاتهای سوم فلز سنگین نامحلول میشود [18،19،24،127،128]. در حمام فسفاته روی، این تعادلها ممکن است به صورت زیر نشان داده شود:
Zn(H2PO4)2 ↔ ZnHPO4 + H3PO4 , (2)
3ZnHPO4 ↔ Zn3(PO4)2 + H3PO4 . (3)
مقداری اسید فسفریک آزاد باید وجود داشته باشد تا هیدرولیز را مهار کند و حمام را برای رسوب موثر فسفات در میکروکاتدها پایدار نگه دارد. عامل دیگری که بر تغییر تعادل بین فسفات اولیه و سوم تأثیر میگذارد، دمای حمام است. دمای بالاتر رسوب آسانتر فسفاتهای سوم را در زمان کوتاهتری تسهیل میکند. از این رو، مقدار بیشتری اسید فسفریک برای حمامهایی که در دمای بالاتر کار میکنند، مورد نیاز است. در مقابل، در مورد حمامهای فسفاته که در دمای اتاق کار میکنند، احتمال افزایش اسیدیته در طول عملیات مداوم بیشتر است [129،130] و معمولاً با افزودن کربنات فلزی که پوشش را تشکیل میدهد (Zn(CO3)2 در حمام فسفاته روی) خنثی میشود. از این رو، بسته به دمای کار و غلظت اجزای موجود در حمام، باید مقدار اسید فسفریک آزاد را برای حفظ شرایط تعادل انتخاب کرد. مقدار بیش از حد اسید فسفریک نه تنها تشکیل پوشش را به تأخیر میاندازد، بلکه منجر به از دست دادن بیش از حد فلز نیز میشود.
در عمل، واکنش فسفاته کردن به دلیل قطبش ناشی از هیدروژن آزاد شده در واکنش کاتدی، تمایل به کندی دارد. برای دستیابی به تشکیل پوشش در زمان عملی، باید از برخی روشهای شتابدهی استفاده شود. اهمیت شتابدهی فرآیند فسفاته کردن در قرن نوزدهم احساس شد و توسعه آن با ظهور فرآیند بوندرید در سال 1929 شتاب زیادی گرفت. اخیراً، Sankara Narayanan و همکاران [131] مروری بر شتابدهی فرآیند فسفاته کردن انجام دادهاند و نقش آن را در تقاضای رو به رشد برای کاهش زمان فرآیند توجیه کردهاند. روشهای مختلف شتابدهی تشکیل پوششهای فسفات را میتوان به طور کلی به سه دسته تقسیم کرد: (i) شتابدهی شیمیایی؛ (ii) شتابدهی مکانیکی؛ و (iii) شتابدهی الکتروشیمیایی.

3.3.1. شتابدهی شیمیایی
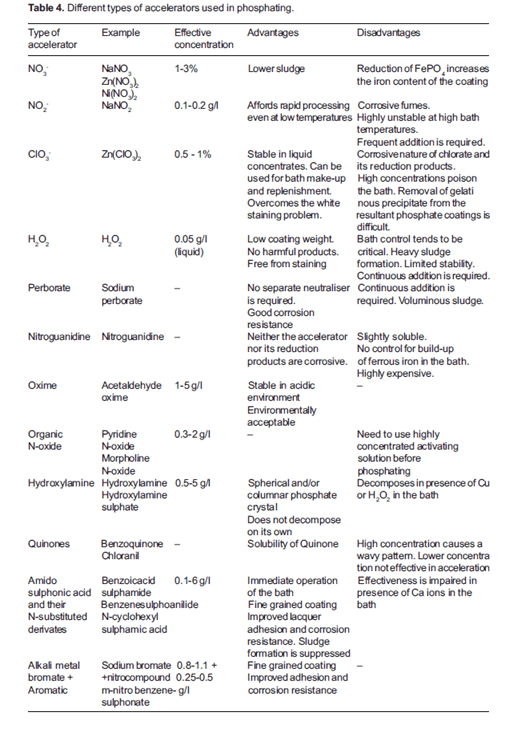
مواد اکسیدکننده [132،133] و فلزات نجیبتر از آهن مانند مس، نیکل [19] و غیره، مهمترین دسته شتابدهندههای شیمیایی را تشکیل میدهند. آنها فرآیند رسوب را از طریق مکانیسمهای مختلف شتاب میدهند. عوامل اکسیدکننده واکنش نیمسل کاتدی را با جلوگیری از تجمع هیدروژن در محلهای کاتدی، دپلاریزه میکنند، در حالی که یونهای فلزات نجیب با رسوب خود، محلهای کاتدی با پتانسیل بیشنقطه کم را فراهم میکنند و در نتیجه انحلال فلز را تقویت میکنند [134]. از آنجایی که شتابدهی از طریق دپلاریزاسیون نسبت به صرفاً تقویت انحلال فلز ترجیح داده میشود، عوامل اکسیدکننده کاربرد گستردهتری نسبت به فلزات پیدا کردهاند. علاوه بر این، آنها از تجمع بیش از حد آهن در حمام جلوگیری میکنند که میتواند برای تشکیل پوشش خوب مضر باشد [25]. شایعترین شتابدهندههای اکسیدکننده مورد استفاده نیتریتها، کلراتها، نیتراتها، پراکسیدها و ترکیبات نیترو آلی به تنهایی یا در ترکیبهای مختلف هستند. ترکیبات رایج نیتریت-نیترات، نیتریت-کلرات-نیترات و کلرات-اسید سولفونیک نیتروبنزن هستند. ویژگیهای برخی از شتابدهندههای اکسیدکننده رایج در جدول 4 آورده شده است.
برخی از عوامل احیاکننده مانند سولفیتهای فلزات قلیایی [135]، هیپوفسفیتها [136]، فسفیتها [137]، فرمالدهید، بنزآلدئید، هیدروکسیلامین [138]، استالدئید اگزیم [139]، پیریمیدین N-اگزیم [140]، مورفولین N-اگزیم [140]، کینونها [141] و غیره نیز به عنوان شتابدهنده آزمایش شدهاند اما از نظر صنعتی به اندازه شتابدهندههای اکسیدکننده موفق نبودهاند.
3.3.2. شتابدهی مکانیکی
هنگامی که یک محلول فسفاته با فشار روی سطح فلزی اسپری میشود، پوششها سریعتر از غوطهوری در همان محلول تشکیل میشوند، زیرا فرآیند اول تأخیر ناشی از انتشار اجزای محلول به سطح فلز را از بین میبرد. سینتیک مقایسهای اسپری و غوطهوری فسفاته توسط Laukonis [142] تعیین شد. پوششهای حاصل نازک، ریزدانه و کاملاً مناسب به عنوان پایه رنگ هستند. سایر روشهای شتابدهی فیزیکی، عمل برسها و غلتکها [143] روی سطح در طول فرآیند است.
3.3.3. شتابدهی الکتروشیمیایی
روشهای الکتروشیمیایی مختلفی برای شتابدهی، هم آندی، هم کاتدی و هم روش پالسی، در ادبیات توصیف شده است [144-161]. کاسلت در سال 1909 توسط کاسلت [144] شتابدهی فرآیند فسفاته کردن را با استفاده از روش کاتدی تشخیص داد. مطالعات بعدی نشان میدهد که روشهای آندی مناسبتر و سودمندتر از روشهای کاتدی هستند، زیرا آنها هم انحلال فلز و هم پاسیواسیون را تقویت میکنند. Zantout و Gabe [148] ادعا میکنند که با اعمال جریان کوچک، به وزن پوشش بالاتر با تخلخل کم در زمان درمان کوتاهتر دست یافتهاند. Ravichandran و همکاران [157-159] کاربرد کوپلینگ گالوانیک زیرلایه فولادی با فلزات نجیبتر از فولاد را برای شتابدهی فرآیندهای فسفاته کردن تثبیت کردند. این روش از اصل خوردگی گالوانیک برای شتابدهی واکنش انحلال فلز استفاده میکند که منجر به مصرف سریعتر اسید فسفریک آزاد و دستیابی زودتر به نقطه شروع رسوب میشود و در نتیجه مقدار بیشتری از تشکیل پوشش فسفات را به همراه دارد. کاربرد جریان کاتدی برای تشکیل پوشش فسفات بر روی فولاد ضد زنگ با استفاده از حمام فسفاته روی اصلاح شده با کلسیم توسط Bjerrum و همکاران [160] ثبت اختراع شده است. سینها و فسر [161] نیز تشکیل پوشش فسفات بر روی زیرلایههای فولادی و فولاد ضد زنگ را با این روش مطالعه کردهاند.
این سه روش شتابدهی که در بالا توضیح داده شد، به طور گسترده در صنایع مورد استفاده قرار میگیرند؛ اما هر کدام مزایا و معایب خاص خود را دارند. اگرچه شتابدهندههای شیمیایی (به ویژه نوع اکسیدکننده) با افزودن ساده خود فرآیند فسفاته کردن را شتاب میدهند، غلظت آنها در حمام برای دستیابی به نتایج مطلوب بسیار حیاتی است. شتابدهی با روشهای مکانیکی محدود به فرآیندهای اسپری است که قادر به تأمین مداوم محلول تازه حمام هستند. روشهای الکتروشیمیایی شتابدهی اگرچه قادر به دستیابی به سرعت رسوب بالاتر هستند، اما مشکل عملی در افزودن “برق” به مرحله پردازش، آن را کمتر محبوب میکند.
سینتیک فرآیند فسفاته کردن مراحل درگیر در طول فسفاته کردن و سرعت آنها را نشان میدهد. تاکنون از سه روش مختلف برای بررسی سینتیک تشکیل پوششهای فسفات استفاده شده است: (i) روش وزنسنجی، با تعیین کمی مقدار فسفات رسوب شده در واحد زمان؛ (ii) روش الکتروشیمیایی بر اساس تعیین نواحی آزاد و واکنشپذیر بدون پوشش از طریق پاسیواسیون الکتروشیمیایی؛ و (iii) روش رادیوگرافی بر اساس تعیین شدت پرتو ایکس مشخصه ترکیب حاصل.
هر سه روش تصویر مشابهی از فرآیند فسفاته کردن ارائه دادند که نشان داد تشکیل پوشش به صورت خطی انجام نمیشود، بلکه در ابتدا بسیار سریع است و پس از آن سرعت با گذشت زمان به آرامی کاهش مییابد.
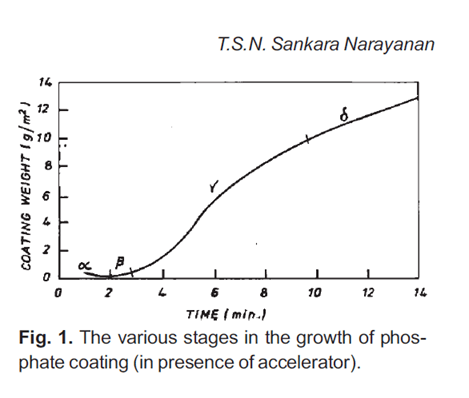
مطالعات در مورد سینتیک فسفاته کردن نشان میدهد که چهار مرحله متمایز در تشکیل پوشش وجود دارد (شکل 1)، یعنی مرحله القایی (a)، شروع رشد فیلم (b)، مرحله رشد نمایی اصلی (g) و مرحله افزایش خطی در رشد فیلم (d). در طول دوره القا، فیلم اکسید باقیمانده روی سطح حتی پس از تمیز کردن حذف میشود. هنگامی که رشد فیلم آغاز میشود، اولین هستهها تشکیل میشوند و سرعت هستهزایی با زمان به سرعت افزایش مییابد. با این حال، این امر به میزان قابل توجهی به شرایط سطح، روشهای پیشپردازش اتخاذ شده و عوامل اکسیدکننده موجود در حمام فسفاته بستگی دارد. رشد در مرحله رشد نمایی اصلی رخ میدهد. افزودن شتابدهندهها دوره القا را کاهش میدهد و مرحله رشد خطی را گسترش میدهد.
به نظر Gebhardt [162]، سرعت فسفاته کردن به سرعت انتشار یونهای Fe2+ از شبکه ساختاری به رابط پوشش/محلول از طریق پوشش تشکیل شده بستگی دارد. Machu [25] دریافت که سرعت واکنش فسفاته کردن تابعی از میکروآندهای روی سطح است.
-dFA/dt = K.FA dt
که در آن dt تغییر در زمان؛ FA سطح آندها در میکروسلها؛ و K ثابت سرعت واکنش.
سرعت تشکیل پوشش فسفات در درجه اول به فلز بستگی دارد، یعنی نسبت سطح آند که در ابتدا وجود داشت، FAo، به سطح آند در هر لحظه، FA. تأثیر عوامل مختلف دیگر که بر سرعت واکنش کنترل دارند، مانند دما، شرایط سطح و غیره، در مقدار ثابت سرعت K منعکس میشود که برای فرآیندهای مختلف متفاوت است.
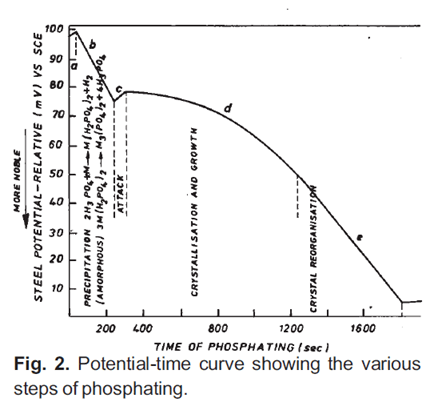
کل فرآیند رشد پوشش را میتوان با منحنیهای پتانسیل-زمان (شکل 2) دنبال کرد که مراحل مختلف پوشش را نشان میدهد و علاوه بر آن نشان میدهد که فسفاته کردن موثر چه زمانی متوقف شده است.
همبستگی روابط پتانسیل-زمان با خواص فیلم به این نتیجه منجر میشود که تشکیل پوشش از طریق مراحل زیر پیش میرود:
(الف) حمله الکتروشیمیایی به فولاد؛ (ب) رسوب آمورف؛ (ج) انحلال فلز پایه؛ (د) تبلور و رشد؛ و (ه) بازآرایی بلوری.
اما در عمل، شناسایی مراحل “ب” و “ج” دشوار است و منحنی عمدتاً فرآیند انحلال فلز، تشکیل پوشش و تکمیل پوشش را نشان میدهد. استفاده از اندازهگیریهای پتانسیل-زمان برای نظارت بر فرآیند فسفاته کردن برای اولین بار توسط Machu [25] توصیف شد. همچنین توسط چندین محقق برای آشکار کردن ماهیت فرآیند در طول فسفاته کردن [145] و خواص پوشش تشکیل شده [163] استفاده شده است. Sankara Narayanan و همکاران [164،165] در مورد مفید بودن منحنیهای پتانسیل-زمان در پیشبینی سینتیک فرآیند فسفاته کردن بحث کردهاند. همچنین کاربرد اندازهگیری پتانسیل-زمان برای نظارت موثر آنلاین بر فرآیند فسفاته کردن نیز ثابت شده است [166،167]. همبستگی بین وزن پوشش و اندازهگیریهای زمان پتانسیل توسط Sankara Narayanan [168-170] برقرار شده است که محاسبه سینتیک تبلور را از اندازهگیری زمان پتانسیل امکانپذیر میکند.
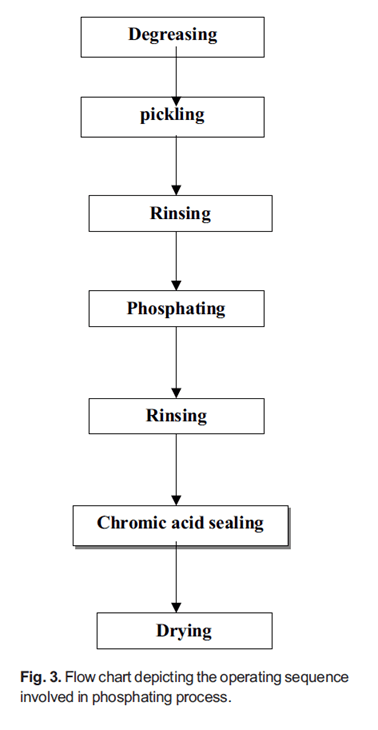
به طور کلی، توالی فسفاته کردن شامل هفت عملیات است، همانطور که در نمودار جریان نشان داده شده است. با این حال، بسته به شرایط سطح فلز پایه، ممکن است برخی از این عملیات حذف شوند یا عملیات اضافی به سیستم اضافه شود. یک توالی هفت مرحلهای معمولی از فرآیند پیشتیمار فسفاته در شکل 3 نشان داده شده است.
3.5.1. تمیزکاری
شاید مهمترین نیازمندی برای تشکیل صحیح پوشش، یک زیرلایه تمیز و عاری از آلودگیهایی مانند روغن، گریس، موم، محصولات خوردگی و سایر آلودگیها باشد. بسیاری از خرابیهای پوشش را میتوان به آمادهسازی ضعیف سطح فلز نسبت داد [171]. یک پاککننده ایدهآل آن است که قادر به حذف تمام آلودگیها از سطح فلز باشد و از رسوب مجدد آنها یا تشکیل سایر محصولات واکنش مضر جلوگیری کند [172]. از روشهای مختلفی مانند سندبلاست، چربیزدایی با حلال، چربیزدایی بخار، تمیزکاری قلیایی و ترشیکاری برای دستیابی به این هدف استفاده شده است.
سندبلاست یک روش موثر برای تمیزکاری مکانیکی است. با این حال، بسیار گران است و استفاده از آن به عنوان یک روش میدانی توجیه میشود که در آن نمیتوان از روشهای شیمیایی استفاده کرد و لازم است پوستههای شل و همچنین رنگ را نیز حذف کرد [173].
حلالهای آلی به طور گسترده برای حذف آلودگیهای آلی از زیرلایههای فلزی استفاده میشوند. اما آنها سمی و قابل اشتعال هستند و نیاز به استفاده در مقادیر زیاد دارند که از نظر اقتصادی مقرون به صرفه نیست. این امر منجر به جایگزینی آن با تکنیک چربیزدایی بخار شده است. مزیت منحصر به فرد تکنیک دوم نسبت به چربیزدایی حلال این است که تمیزکاری مداوم با مقادیر کمی حلال امکانپذیر است [174].
تمیزکاری قلیایی جایگزین اقتصادی و موثری برای استفاده از حلالهای آلی برای حذف گریس، روغن و موم است. آنها همچنین همراه با مواد فعال سطحی (مرطوبکننده) و حلالهای هیدروکربنی امولسیون شده استفاده میشوند [174]. پاککنندههای قلیایی به ویژه در هنگام استفاده گرم (تقریباً 79 درجه سانتیگراد) کارآمد هستند. در حالی که تمیزکاری قلیایی عاری از خطرات آتشسوزی و سمیت مرتبط با تمیزکاری حلالهای آلی است (مگر اینکه حلالهای امولسیون شده گنجانده شده باشند)، باید از اثرات خورنده مواد قلیایی بر روی پوست و لباسهای معمولی محافظت کرد. به ویژه سود سوزآور میتواند باعث سوختگی شدید پوست و چشم شود و در صورت استنشاق بسیار برای غشاهای بینی و برونش تحریککننده است.
تمیزکاری اسیدی یا ترشیکاری با استفاده از اسیدهایی مانند HCl، H2SO4 و H3PO4 یک روش بسیار موثر برای حذف زنگزدگی و پوستههای آسیاب است [175]. محلولهای رقیق (5-10 درصد وزنی) H2SO4 و HCl در حضور بازدارندهها برای حذف آلودگیهای معدنی با تبدیل آنها به نمکهای آهن استفاده میشوند. ترشیکاری در H2SO4 معمولاً در دمای بالا (حدود 60 درجه سانتیگراد) انجام میشود. H3PO4 یک عامل تمیزکننده عالی و آزمایششده در زمان است که نه تنها آلودگیهای آلی و معدنی موجود روی فلز را حذف میکند، بلکه با واکنش با آن برای تولید یک سطح مکانیکی و شیمیایی پذیرنده برای تشکیل پوشش بعدی، باعث حکاکی شیمیایی سطح میشود [176].
ترشیکاری الکترولیتی جایگزینی برای ترشیکاری شیمیایی است که تمیزکاری بهتر و سریعتری را از طریق افزایش تکامل هیدروژن فراهم میکند که منجر به افزایش تلاطم و عمل انفجاری میشود [174].
تمامی حقوق مادی و معنوی این وبسایت، متعلق به FYP میباشد.
طراحیشده توسط آژانس دیجیتال مارکتینگ HDM